风湿病
2011-10-21 14:18:57 来源: 作者: 评论:0 点击:
风湿病(rheumatism)是一种与A组β溶血性链球菌感染有关的的变态反应性疾病。病变主要累及全身结缔组织,呈急性或慢性结缔组织炎症,胶原纤维发生纤维素样变性。本病为结缔组织病(connective tissue disease)即胶原病的一种。心脏、关节和血管最常被累及,以心脏病变最为严重。急性期称为风湿热(rheumatic fever),临床上,除有心脏和关节症状外,常伴有发热、毒血症、皮疹、皮下结节、舞蹈症等症状和体征;血液检查,抗链球菌溶血素O抗体滴度增高,血沉加快等。
本病可发生于任何年龄,但多始发于5~14岁儿童,发病高峰为6~9岁。常反复发作,急性期过后,可造成轻重不等的心瓣膜器质性病变。
风湿病多发生于寒冷地区,热带地区少见。在我国,以东北和华北发病较多,是一种常见病。
一、病因和发病机制
风湿病的病因和发病机制尚未完全明了,但其发生与A组β溶血性链球菌的感染有关。本病多发生于寒冷地区,与链球菌感染盛行地区一致。冬、春季气候寒冷而潮湿,易发生急性扁桃体炎、咽峡炎,从而导致风湿病。抗生素的广泛应用不但能预防和治疗咽峡炎、扁桃体炎,而且明显地减少风湿病的发生和复发。
近来研究证明:A组溶血性链球菌胞壁的成分中,M-蛋白和C-多糖具有特异的抗原性。此外,A组溶血性链球菌能产生一些酶,亦具有抗原性,并能破坏相应的底物,如链球菌溶血素O(能分解血红蛋白)、链激酶能激活血中纤维蛋白溶酶原,使之变为纤维蛋白溶酶(分解纤维蛋白)、链球菌透明质酸酶(分解透明质酸)、链道酶(能分解DNA)及链球菌烟酰胺腺嘌呤二核苷酸酶。此外,还能产生链球菌溶血素S(SLS,为脂蛋白,抗原性微弱)。在链球菌感染时,初次接触抗原后约7~10天,即有抗体形成。在急性风湿性关节炎时,在咽峡炎初次发作后10~15天,患者血清抗链球菌抗体滴度明显升高。至今,临床上仍以检测抗链球菌溶血素O作为诊断指标(滴度1:500单位以上为阳性)。
发病机制有以下学说:①链球菌感染学说:认为本病是链球菌直接感染所致,但从病灶中均未能检测或分离出链球菌。②链球菌毒素学说:认为病变是由链球菌毒素(如SLS、SLO、链球菌蛋白酶、C-多糖等)所引起。③变态反应学说:认为病变是由于机体对链球菌抗原产生超敏反应(主要为Ⅲ型变态反应常伴有血内补体减少,两者均不见于风湿热。而且,几乎不能解释Aschoff小体的发生。④自身免疫学说:目前支持者最多。大多数风湿热患者可证明有对心内膜(或心肌原纤维)、平滑肌(如血管壁)、心内膜等起反应的自身抗体。再者,已证明链球菌与组织成分之间存在交叉反应,即M-蛋白与心肌抗原之间(将M-蛋白注射于动物体内,产生的抗体可与心肌内膜起反应)链球菌多糖与心肌糖蛋白之间,以及链球菌透明质酸与软骨的蛋白多糖复合物之间的交叉反应。在活动性风湿性全心炎患者,免疫荧光检查证明,心肌内有弥漫的免疫球蛋白沉积;心瓣膜(主要在闭锁缘)有IgG沉积,然而是否有自身抗体性质尚无定论。总之,体液因素(Ⅲ型超敏反应、自身免疫)、细胞介导免疫及毒素作用都可能参与发病环节。
二、基本病变
风湿热时,病变可累及全身结缔组织,特别是心脏各层均可被累及;小动脉亦往往被侵犯。病变发展过程大致可分为三期:
1.变质渗出期开始是结缔组织纤维发生粘液样变性,可见胶原纤维肿胀(原纤维间水肿,intermicrofibrillary edema),结缔组织基质内蛋白多糖(主要为氨基葡聚糖)增多。HE染色呈嗜碱性,甲苯胺蓝染色呈异染性,即呈红色。继而肿胀的胶原纤维断裂、崩解成无结构的颗粒状物,与基质中的氨基葡聚糖混合在一起,加上免疫球蛋白、有时还有纤维蛋白沉积,致使病灶的染色性状颇似纤维蛋白,因此称为纤维素样变性(纤维素样坏死)。此外,病灶中还有少量浆液和炎症细胞(淋巴细胞、个别中性粒细胞和单核细胞)浸润。此期持续约1个月。
2.增生期 亦称为肉芽肿期(granulomatous phase ),其特点是形成具有疾病特征性的风湿性肉芽肿,即Aschoff小体(Aschoff body),对本病具有诊断意义。
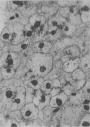
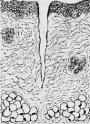
Aschoff 小体体积颇小,一般显微镜下才能看见(图8-19),多发生于心肌间质、心内膜下和皮下结缔组织;心外膜、关节和血管等处少见。在心肌间质内者多位于小血管旁,略带圆形或梭形,其中心部为纤维素样坏死灶,周围有各种细胞成分:①Anitschkow细胞:胞浆丰富,嗜碱性,核大,呈卵圆形、空泡状。染色质集中于核的中央,核的横切面状似枭眼;纵切面上,染色质状如毛虫。②Aschoff巨细胞(Aschoff giant cell):含有1~4个泡状的核,与Anitschkow细胞相似,胞浆嗜碱性。以上两种细胞的来源尚有争论,但现代标记技术证明其为巨噬细胞源性。③小体内还有少量淋巴细胞(主要为T细胞)和个别中性粒细胞。此期经过约2~3个月。

图8-19 Aschoff小体
主由Anitschkow细胞、Aschoff巨细胞和淋巴细胞等组成,中心部常有纤维素样坏死物
3.瘢痕期(愈合期) 细胞成分减少,出现纤维母细胞,产生胶原纤维,并变为纤维细胞。整个小体变为梭形小瘢痕。此期经过约2~3个月。
本病病变的自然经过为4~6个月,但常反复发作,因此,新旧病变常同时并存。
发生在浆膜的风湿病变主要为浆液性和(或)纤维素性炎症。
三、各器官的病变
(一)风湿性心脏病
风湿病时病变常累及心脏各层,故称为风湿性全心炎(rheumatic pancarditis)。
1.风湿性心内膜炎 风湿性心内膜炎(rheumatic endocarditis)常侵犯心瓣膜,其中二尖瓣最常被累及,其次为二尖瓣和主动脉瓣同时受累。三尖瓣和肺动脉瓣一般不被累及。腱索和左心房壁内膜有时也可被侵犯。
病变早期表现为浆液性心内膜炎,瓣膜肿胀、透亮,但尸检时这种早期变化几乎看不到。镜下,瓣膜因浆液性渗出物而变得疏松,伴有巨噬细胞的游入,胶原纤维发生纤维素样坏死。其后,坏死灶周围出现Anitschkow细胞,严重病例可有Aschoff小体形成(图8-20)。几周后,在瓣膜闭锁缘上有单行排列的,直径为1~2mm的疣状赘生物(verrucous vegetation)。此种心内膜炎又称为疣状心内膜炎(verrucous endocarditis)。这些疣赘物呈灰白色半透明,附着牢固,一般不易脱落(图8-21)。镜下,疣赘物为由血小板和纤维素构成的白色血栓。疣赘物主要发生于二尖瓣的心房面和主动脉瓣心室面,其原因:由于瓣膜炎症波及内皮细胞使之受损伤,同时由于心瓣膜不停地关闭和启开,闭锁缘处内膜经常受到摩擦和血流冲击,使受损内皮细胞脱落,内皮下胶原裸露,因而导致血栓形成。有时,左心房壁亦有血栓形成。

图8-20 风湿性心内膜炎
心内膜切片上见增生的细胞呈栅状排列并有Aschoff小体形成 ×80

图8-21 风湿性疣状心内膜炎
二尖瓣和主动脉瓣闭锁缘见呈单行排列整齐的细小疣赘物
病变后期,心内膜下病灶发生纤维化,疣赘物亦发生机化。由于风湿病常反复发作,瘢痕形成越来越多。心壁内膜可增厚、粗糙和皱缩,尤以左心房后壁更为显著,称为McCallum斑(McCallum’s patch)。
心瓣膜由于病变反复发作和机化,大量结缔组织增生,致使瓣膜增厚、卷曲、缩短以及钙化,瓣叶之间可发生粘连和纤维性愈着,腱索增粗和缩短,终致形成慢性心瓣膜病(图8-22)。

图8-22 风湿性二尖瓣瓣膜病
瓣膜增厚、变形,瓣叶粘连,腱索增粗、缩短。左心房显著扩张
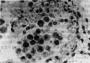
2.风湿性心肌炎 风湿性心肌炎(rheumatic myocarditis)主要累及心肌间质结缔组织。心肌小动脉近旁的结缔组织发生纤维素样坏死,继而形成Aschoff小体(图8-23)。小体呈弥漫性或局限性分布,大小不一,多呈梭形,最常见于左心室后壁、室间隔、左心房及左心耳等处。后期,小体发生纤维化,形成梭形小瘢痕。

图8-23 风湿性心肌炎
心肌间质中血管旁可见群集的Anitschkow细胞(Aschoff小体),小体已有部分纤维化。右下角为Anitschkow细胞的高倍放大照片,其核状似枭眼
有时在儿童,渗出性病变特别明显,心肌间质发生明显水肿及弥漫性炎性细胞浸润。严重者常引起心功能不全。
风湿性心肌炎常可影响心肌收缩力,临床上表现为心搏加快,第一心间低钝,严重者可导致心功能不全。心电图常见P-R间期延长,可能是由于病变波及房室结或迷走神经兴奋所致。
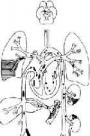
3.风湿性心包炎 风湿病时,心包几乎总被累及,但临床上,仅15%的风湿性心包炎(rheumatic pericarditis)病例被确诊。病变主要累及心包脏层,呈浆液性或浆液纤维素性炎症,心外膜结缔组织可发生纤维素样变性。心包腔内可有大量浆液渗出(心包积液)。叩诊心界向左、右扩大,听诊时心音遥远,X线检查,心脏呈梨形。当有大量纤维蛋白渗出时,心外膜表面的纤维素因心脏的不停搏动而成绒毛状,称为绒毛心(cor villosum)(图8-24)。恢复期,浆液逐渐被吸收,纤维素亦大部被溶解吸收,少部分发生机化,致使心包的脏、壁两层发生部分粘连,极少数病例可完全愈着,形成缩窄性心包炎(consrictive pericarditis)。

图8-24 风湿性心外膜炎
心外膜上覆盖一层纤维素性假膜,呈绒毛状(绒毛心)
(二)风湿性关节炎
约75%风湿热患者早期出现风湿性关节炎(rheumatic arthritis)。常累及大关节,最常见于膝和踝关节,其次是肩、腕、肘等关节。各关节常先后受累,反复发作,局部出现红、肿、热、痛和功能障碍。镜下,病变主要为浆液性炎,并有少量淋巴细胞和纤维素渗出,有时在关节周围结缔组织内可有少数Aschoff小体形成。愈复时,浆液性渗出物被完全吸收,一般不留后遗症。
(三)风湿性动脉炎
风湿性动脉炎(rheumatic arteritis)可发生于冠状动脉、肾动脉、肠系膜动脉、脑动脉、主动脉和肺动脉等。急性期,血管壁发生粘液样变性和纤维素样坏死,伴有炎症细胞浸润,可有Aschoff小体形成,并可继发血栓形成。后期,血管壁因瘢痕形成而呈不规则增厚,管腔狭窄。
(四)皮肤病变
渗出性病变:躯干和四肢皮肤出现环形红斑(erythema annulare),为环形或半环形淡红色斑,1~2日可消退,发生于风湿热的急性期,对急性风湿病有诊断意义。镜下,红斑处真皮浅层血管充血,血管周围水肿及炎性细胞浸润。
增生性病变:皮下结节(subcutaneous nodules)多见于肘、腕、膝、踝关节附近伸侧面皮下,直径0.5~2cm,圆形或椭圆形,质地较硬,活动,压之不痛。镜下,结节中心为大片纤维素样坏死物质,其周围可见增生的纤维母细胞和Anitschkow细胞呈栅状排列,伴有炎性细胞(主要为淋巴细胞)浸润。数周后,结节逐渐纤维化而变为瘢痕组织。风湿热时,皮下结节并不经常出现,但有诊断意义。
(五)中枢神经系统病变
多见于5~12岁儿童,女孩多于男孩。主要病变为风湿性动脉炎,可有神细胞变性、胶质细胞增生及胶质结节形成。病变主要累及大脑皮质、基底节、丘脑及小脑皮层。当锥体外系统受累较重时,患儿出现肢体的不自主运动,称为小舞蹈症(chorea minor)。
本病可发生于任何年龄,但多始发于5~14岁儿童,发病高峰为6~9岁。常反复发作,急性期过后,可造成轻重不等的心瓣膜器质性病变。
风湿病多发生于寒冷地区,热带地区少见。在我国,以东北和华北发病较多,是一种常见病。
一、病因和发病机制
风湿病的病因和发病机制尚未完全明了,但其发生与A组β溶血性链球菌的感染有关。本病多发生于寒冷地区,与链球菌感染盛行地区一致。冬、春季气候寒冷而潮湿,易发生急性扁桃体炎、咽峡炎,从而导致风湿病。抗生素的广泛应用不但能预防和治疗咽峡炎、扁桃体炎,而且明显地减少风湿病的发生和复发。
近来研究证明:A组溶血性链球菌胞壁的成分中,M-蛋白和C-多糖具有特异的抗原性。此外,A组溶血性链球菌能产生一些酶,亦具有抗原性,并能破坏相应的底物,如链球菌溶血素O(能分解血红蛋白)、链激酶能激活血中纤维蛋白溶酶原,使之变为纤维蛋白溶酶(分解纤维蛋白)、链球菌透明质酸酶(分解透明质酸)、链道酶(能分解DNA)及链球菌烟酰胺腺嘌呤二核苷酸酶。此外,还能产生链球菌溶血素S(SLS,为脂蛋白,抗原性微弱)。在链球菌感染时,初次接触抗原后约7~10天,即有抗体形成。在急性风湿性关节炎时,在咽峡炎初次发作后10~15天,患者血清抗链球菌抗体滴度明显升高。至今,临床上仍以检测抗链球菌溶血素O作为诊断指标(滴度1:500单位以上为阳性)。
发病机制有以下学说:①链球菌感染学说:认为本病是链球菌直接感染所致,但从病灶中均未能检测或分离出链球菌。②链球菌毒素学说:认为病变是由链球菌毒素(如SLS、SLO、链球菌蛋白酶、C-多糖等)所引起。③变态反应学说:认为病变是由于机体对链球菌抗原产生超敏反应(主要为Ⅲ型变态反应常伴有血内补体减少,两者均不见于风湿热。而且,几乎不能解释Aschoff小体的发生。④自身免疫学说:目前支持者最多。大多数风湿热患者可证明有对心内膜(或心肌原纤维)、平滑肌(如血管壁)、心内膜等起反应的自身抗体。再者,已证明链球菌与组织成分之间存在交叉反应,即M-蛋白与心肌抗原之间(将M-蛋白注射于动物体内,产生的抗体可与心肌内膜起反应)链球菌多糖与心肌糖蛋白之间,以及链球菌透明质酸与软骨的蛋白多糖复合物之间的交叉反应。在活动性风湿性全心炎患者,免疫荧光检查证明,心肌内有弥漫的免疫球蛋白沉积;心瓣膜(主要在闭锁缘)有IgG沉积,然而是否有自身抗体性质尚无定论。总之,体液因素(Ⅲ型超敏反应、自身免疫)、细胞介导免疫及毒素作用都可能参与发病环节。
二、基本病变
风湿热时,病变可累及全身结缔组织,特别是心脏各层均可被累及;小动脉亦往往被侵犯。病变发展过程大致可分为三期:
1.变质渗出期开始是结缔组织纤维发生粘液样变性,可见胶原纤维肿胀(原纤维间水肿,intermicrofibrillary edema),结缔组织基质内蛋白多糖(主要为氨基葡聚糖)增多。HE染色呈嗜碱性,甲苯胺蓝染色呈异染性,即呈红色。继而肿胀的胶原纤维断裂、崩解成无结构的颗粒状物,与基质中的氨基葡聚糖混合在一起,加上免疫球蛋白、有时还有纤维蛋白沉积,致使病灶的染色性状颇似纤维蛋白,因此称为纤维素样变性(纤维素样坏死)。此外,病灶中还有少量浆液和炎症细胞(淋巴细胞、个别中性粒细胞和单核细胞)浸润。此期持续约1个月。
2.增生期 亦称为肉芽肿期(granulomatous phase ),其特点是形成具有疾病特征性的风湿性肉芽肿,即Aschoff小体(Aschoff body),对本病具有诊断意义。
Aschoff 小体体积颇小,一般显微镜下才能看见(图8-19),多发生于心肌间质、心内膜下和皮下结缔组织;心外膜、关节和血管等处少见。在心肌间质内者多位于小血管旁,略带圆形或梭形,其中心部为纤维素样坏死灶,周围有各种细胞成分:①Anitschkow细胞:胞浆丰富,嗜碱性,核大,呈卵圆形、空泡状。染色质集中于核的中央,核的横切面状似枭眼;纵切面上,染色质状如毛虫。②Aschoff巨细胞(Aschoff giant cell):含有1~4个泡状的核,与Anitschkow细胞相似,胞浆嗜碱性。以上两种细胞的来源尚有争论,但现代标记技术证明其为巨噬细胞源性。③小体内还有少量淋巴细胞(主要为T细胞)和个别中性粒细胞。此期经过约2~3个月。

图8-19 Aschoff小体
主由Anitschkow细胞、Aschoff巨细胞和淋巴细胞等组成,中心部常有纤维素样坏死物
3.瘢痕期(愈合期) 细胞成分减少,出现纤维母细胞,产生胶原纤维,并变为纤维细胞。整个小体变为梭形小瘢痕。此期经过约2~3个月。
本病病变的自然经过为4~6个月,但常反复发作,因此,新旧病变常同时并存。
发生在浆膜的风湿病变主要为浆液性和(或)纤维素性炎症。
三、各器官的病变
(一)风湿性心脏病
风湿病时病变常累及心脏各层,故称为风湿性全心炎(rheumatic pancarditis)。
1.风湿性心内膜炎 风湿性心内膜炎(rheumatic endocarditis)常侵犯心瓣膜,其中二尖瓣最常被累及,其次为二尖瓣和主动脉瓣同时受累。三尖瓣和肺动脉瓣一般不被累及。腱索和左心房壁内膜有时也可被侵犯。
病变早期表现为浆液性心内膜炎,瓣膜肿胀、透亮,但尸检时这种早期变化几乎看不到。镜下,瓣膜因浆液性渗出物而变得疏松,伴有巨噬细胞的游入,胶原纤维发生纤维素样坏死。其后,坏死灶周围出现Anitschkow细胞,严重病例可有Aschoff小体形成(图8-20)。几周后,在瓣膜闭锁缘上有单行排列的,直径为1~2mm的疣状赘生物(verrucous vegetation)。此种心内膜炎又称为疣状心内膜炎(verrucous endocarditis)。这些疣赘物呈灰白色半透明,附着牢固,一般不易脱落(图8-21)。镜下,疣赘物为由血小板和纤维素构成的白色血栓。疣赘物主要发生于二尖瓣的心房面和主动脉瓣心室面,其原因:由于瓣膜炎症波及内皮细胞使之受损伤,同时由于心瓣膜不停地关闭和启开,闭锁缘处内膜经常受到摩擦和血流冲击,使受损内皮细胞脱落,内皮下胶原裸露,因而导致血栓形成。有时,左心房壁亦有血栓形成。

图8-20 风湿性心内膜炎
心内膜切片上见增生的细胞呈栅状排列并有Aschoff小体形成 ×80

图8-21 风湿性疣状心内膜炎
二尖瓣和主动脉瓣闭锁缘见呈单行排列整齐的细小疣赘物
病变后期,心内膜下病灶发生纤维化,疣赘物亦发生机化。由于风湿病常反复发作,瘢痕形成越来越多。心壁内膜可增厚、粗糙和皱缩,尤以左心房后壁更为显著,称为McCallum斑(McCallum’s patch)。
心瓣膜由于病变反复发作和机化,大量结缔组织增生,致使瓣膜增厚、卷曲、缩短以及钙化,瓣叶之间可发生粘连和纤维性愈着,腱索增粗和缩短,终致形成慢性心瓣膜病(图8-22)。

图8-22 风湿性二尖瓣瓣膜病
瓣膜增厚、变形,瓣叶粘连,腱索增粗、缩短。左心房显著扩张
2.风湿性心肌炎 风湿性心肌炎(rheumatic myocarditis)主要累及心肌间质结缔组织。心肌小动脉近旁的结缔组织发生纤维素样坏死,继而形成Aschoff小体(图8-23)。小体呈弥漫性或局限性分布,大小不一,多呈梭形,最常见于左心室后壁、室间隔、左心房及左心耳等处。后期,小体发生纤维化,形成梭形小瘢痕。

图8-23 风湿性心肌炎
心肌间质中血管旁可见群集的Anitschkow细胞(Aschoff小体),小体已有部分纤维化。右下角为Anitschkow细胞的高倍放大照片,其核状似枭眼
有时在儿童,渗出性病变特别明显,心肌间质发生明显水肿及弥漫性炎性细胞浸润。严重者常引起心功能不全。
风湿性心肌炎常可影响心肌收缩力,临床上表现为心搏加快,第一心间低钝,严重者可导致心功能不全。心电图常见P-R间期延长,可能是由于病变波及房室结或迷走神经兴奋所致。
3.风湿性心包炎 风湿病时,心包几乎总被累及,但临床上,仅15%的风湿性心包炎(rheumatic pericarditis)病例被确诊。病变主要累及心包脏层,呈浆液性或浆液纤维素性炎症,心外膜结缔组织可发生纤维素样变性。心包腔内可有大量浆液渗出(心包积液)。叩诊心界向左、右扩大,听诊时心音遥远,X线检查,心脏呈梨形。当有大量纤维蛋白渗出时,心外膜表面的纤维素因心脏的不停搏动而成绒毛状,称为绒毛心(cor villosum)(图8-24)。恢复期,浆液逐渐被吸收,纤维素亦大部被溶解吸收,少部分发生机化,致使心包的脏、壁两层发生部分粘连,极少数病例可完全愈着,形成缩窄性心包炎(consrictive pericarditis)。

图8-24 风湿性心外膜炎
心外膜上覆盖一层纤维素性假膜,呈绒毛状(绒毛心)
(二)风湿性关节炎
约75%风湿热患者早期出现风湿性关节炎(rheumatic arthritis)。常累及大关节,最常见于膝和踝关节,其次是肩、腕、肘等关节。各关节常先后受累,反复发作,局部出现红、肿、热、痛和功能障碍。镜下,病变主要为浆液性炎,并有少量淋巴细胞和纤维素渗出,有时在关节周围结缔组织内可有少数Aschoff小体形成。愈复时,浆液性渗出物被完全吸收,一般不留后遗症。
(三)风湿性动脉炎
风湿性动脉炎(rheumatic arteritis)可发生于冠状动脉、肾动脉、肠系膜动脉、脑动脉、主动脉和肺动脉等。急性期,血管壁发生粘液样变性和纤维素样坏死,伴有炎症细胞浸润,可有Aschoff小体形成,并可继发血栓形成。后期,血管壁因瘢痕形成而呈不规则增厚,管腔狭窄。
(四)皮肤病变
渗出性病变:躯干和四肢皮肤出现环形红斑(erythema annulare),为环形或半环形淡红色斑,1~2日可消退,发生于风湿热的急性期,对急性风湿病有诊断意义。镜下,红斑处真皮浅层血管充血,血管周围水肿及炎性细胞浸润。
增生性病变:皮下结节(subcutaneous nodules)多见于肘、腕、膝、踝关节附近伸侧面皮下,直径0.5~2cm,圆形或椭圆形,质地较硬,活动,压之不痛。镜下,结节中心为大片纤维素样坏死物质,其周围可见增生的纤维母细胞和Anitschkow细胞呈栅状排列,伴有炎性细胞(主要为淋巴细胞)浸润。数周后,结节逐渐纤维化而变为瘢痕组织。风湿热时,皮下结节并不经常出现,但有诊断意义。
(五)中枢神经系统病变
多见于5~12岁儿童,女孩多于男孩。主要病变为风湿性动脉炎,可有神细胞变性、胶质细胞增生及胶质结节形成。病变主要累及大脑皮质、基底节、丘脑及小脑皮层。当锥体外系统受累较重时,患儿出现肢体的不自主运动,称为小舞蹈症(chorea minor)。
相关热词搜索:
论坛新帖
医学推广
频道本月排行
- 8细胞和组织的适应、损伤与修复
- 5再生
- 5冠状动脉性心脏病
- 4神经系统对损伤的基本反应
- 3血栓形成
- 3动脉炎
- 2感染性疾病
- 2食管疾病
- 2胰腺疾病
- 2滋养层细胞肿瘤
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(11)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)