病历摘要
患者男性,23岁,因“反复浮肿、蛋白尿9个月,腹痛、黑便11天”收入院。
患者于2011月10月无明显诱因出现颜面部浮肿,伴左下腹疼痛、腹泻(水样便,10次/天),我院门诊查血白蛋白(Alb)19.8g/L,血肌酐(Scr)1.13mg/dl,D-二聚体1.30mg/L,尿蛋白定量11.19g/24h,CT血管成像(CTV)提示两下肺肺动脉及分支多发血栓、左肾静脉及下腔静脉内血栓,诊断“肾病综合征,深静脉血栓形成伴肺动脉栓塞”,给予低分子量肝素治疗血栓,泼尼松60mg/d口服治疗原发病,1个月后达完全缓解,复查CTV示下腔静脉及左肾静脉血栓消失,泼尼松规律减量。
2012年1月和4月,患者两次在泼尼松减至40mg/d时肾病复发,均伴恶心、呕吐,脐部右侧隐痛,腹泻、解黄色稀水样便,尿量减少。分别予足量泼尼松、泼尼松加环孢素治疗均能达完全缓解(CR),给予低分子量肝素抗凝、对症治疗后腹部症状均能好转。6月1日,行肾活检术,病理提示“微小病变型IgA肾病”。
2012年7月20日,患者劳累后出现冷汗、心慌,当晚恶心,呕吐胃内容物10余次/天,无咖啡渣样物质、无呕血;全腹持续性隐痛,阵发性加剧,伴腹胀、腹泻,黄色、糊状便,3次/天,间断少量黑色稀便。27日至我院,查Alb23.7g/L,SCr0.89mg/dl,尿蛋白4+,D-二聚体0.88mg/L,抗凝血酶Ⅲ47.9%;粪便隐血(+),红细胞镜检3~5/高倍镜视野(HP)。29日,解全程鲜红色血便约50ml。
为进一步诊治,于7月30日收入我院。本次复发后患者尿量约300~400ml/d。病程中无皮疹、关节痛、口腔溃疡等不适。精神一般,睡眠尚可,禁食中,体力下降,体重较前增加。5月17日,过敏原检测(食入组):“螨虫”过敏。
体格检查
血压120/100mmHg,体温37℃,脉搏101次/分,呼吸19次/分,颜面、颈项及背部多发痤疮,全腹部、双下肢可见多处紫纹。双眼球结膜水肿。双肺呼吸音清,右下肺呼吸音减低,未闻及音,心率101次/分,律齐,未闻及杂音。腹软,全腹广泛压痛,伴反跳痛,未扪及包块,肝脾肋下未及,腹水征阴性,肠鸣音减弱,双下肢轻度浮肿。
实验室检查
尿液 尿蛋白定量4.28g/24h;N-乙酰-β-D-氨基葡萄糖苷酶(NAG)64.3u/g?cr,视黄醇结合蛋白(RBP)0.5mg/L;急性肾小管损伤标志物:中性粒细胞明胶酶相关脂质运载蛋白(NGAL)136.74μg/L,肾损伤分子1(KIM-1)3.57μg/L,白介素(IL)-18329.45ng/L;无镜下血尿和白细胞尿。
血液血常规:血红蛋白16.2g/dl,白细胞7.9×109/L,中性/淋巴比例79/15,血小板328×109/L。血生化:Alb21.2g/L,球蛋白17.1g/L,尿素氮26.9mg/dl,SCr0.94mg/dl,尿酸416μmol/L,肝酶正常,总胆固醇12.37mmol/L,甘油三酯2.65mmol/L,钾、钠、氯正常,总二氧化碳33.3mmol/L,钙1.82mmol/L,磷1.31mmol/L,C反应蛋白正常,前白蛋白54mg/L。D-二聚体0.52mg/L。体液免疫:IgG0.919g/L,IgE190.0IU/ml,余免疫球蛋白正常。
粪便 粪常规(7月30日至8月2日)黄色稀糊状,隐血阳性,镜检红细胞及白细胞均为0~1/HP;8月3日,解果酱色稀便20ml;8月4日,粪常规为黄色稀糊状便,隐血阴性。
辅助检查
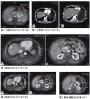
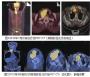
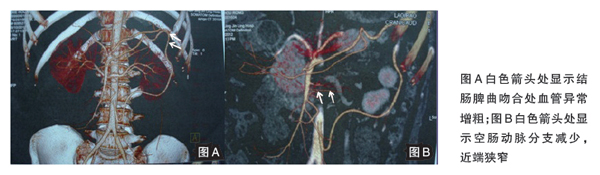
8月2日胃镜见:胃体黏膜光滑,色潮红,未见溃疡;胃窦黏膜红白相间,以红为主,未见溃疡及新生物(活检病理:慢性浅表性胃窦炎),慢性胃炎。8月7日,结肠镜可见:直肠黏膜密集出血点,远端结肠炎。8月13日,行口服适量对比剂(泛影葡胺)与清水混合液后,仰卧位及俯卧位腹部扫描及血管成像提示:腹腔干与肠系膜上动脉共干,且起始处中度狭窄;空肠动脉分支减少,近端狭窄,肠系膜下动脉分支与肠系膜上动脉吻合,以供血空肠、降结肠区域(图A和B);左肾静脉局部充盈缺损,周围可见部分侧枝循环建立,腹腔少量积液;胃-十二指肠-空肠-回肠均显示清晰,未见明显节段性狭窄、扩张及异常沟通区域。8月21日,行经肛小肠镜检查:进镜距回盲部上约200cm,退镜所见黏膜未见明显异常。
诊疗分析
青年男性,慢性病程,肾脏病表现为激素治疗依赖的肾病综合征。患者起病及每次复发时,均合并腹胀、腹痛、腹泻等消化系统症状,本次还合并血便。经抗凝、对症处理,随着肾脏病缓解,消化道症状随之缓解。肾脏病行肾活检诊断为IgA肾病(微小病变型),起病时合并左肾静脉、下腔静脉血栓形成及肺动脉栓塞。根据上述特点,临床须与以下疾病鉴别。
过敏性紫癜 本例患者伴消化系统受累,既往过敏源检查提示对螨虫过敏,激素治疗有效。但病程中始终未出现典型过敏性紫癜样皮疹,反复尿检均无血尿,肾脏病理检查未发现肾小球毛细血管节段襻坏死、新月体形成等常见的血管炎表现,与典型的过敏性紫癜性肾炎的表现不同。肠镜及胃镜亦未见消化道黏膜水肿、溃疡、糜烂等过敏性紫癜消化道黏膜损害表现,因此不支持该病。
克罗恩病 克罗恩病是一种胃肠道慢性炎性肉芽肿性疾病,临床为慢性病程,活动期与缓解期交替,表现为腹痛、腹泻,也可有全身多个系统损害,肠外可累及肾脏,病理类型以IgA肾病多见,糖皮质激素、免疫抑制剂治疗有效,内镜下可见纵行溃疡,溃疡周围黏膜呈鹅卵石样,慢性病变可见肠腔狭窄、炎性息肉等表现。本例患者胃镜、结肠镜、小肠镜检查均未见明显异常,且亦无肠腔狭窄、炎性息肉等慢性化病变,因此不支持克罗恩病诊断。
缺血性肠病 患者的消化道症状随肾病缓解而消失,肾脏病缓解期间消化道症状稳定。肾脏病表现为肾病综合征,血液高凝,起病时有深静脉血栓形成及肺栓塞史,本次复发后腹部增强CT扫描提示腹腔干与肠系膜上动脉共干,且起始处中度狭窄;空肠动脉分支减少,近端狭窄,肠系膜下动脉与肠系膜上动脉分支吻合处较正常为粗。以上均高度提示患者存在肠系膜血管血栓形成或栓塞的高危因素,但影像学检查未找到明确的肠系膜血管血栓形成或栓塞的直接证据,可能与发病时间长、血栓小及受累血管分支小,行CT增强扫描敏感度有限有关。此外,该患者的多种消化内镜检查均未发现黏膜缺血或坏死证据,考虑与其病变轻,缓解快,以及检查时间相对较滞后等有关。虽未找到肠道缺血直接证据,但从临床及影像学间接证据考虑,及排除其他可能疾病后,均支持缺血性肠病的诊断。
诊疗经过及转归
予甲泼尼龙40mg/d静滴治疗原发病,禁食、肠外营养、泮托拉唑护胃治疗消化道症状,同时间断输注血浆加强支持治疗,1周后消化道症状缓解,半月后复查尿蛋白降至0.49g/24h,改泼尼松50mg/d口服出院。
最后诊断:①IgA肾病(微小病变型);②缺血性肠病。
分析与讨论
缺血性肠病是肠壁血液灌注不良引起的肠壁缺血性疾病,可累及各段消化道,常见于结肠,可分为急性肠系膜缺血(AMI)、慢性肠系膜缺血(CMI)及缺血性结肠炎(IC)。该病发病率低,早期患者无特异性表现,很容易误诊。国内孙丹莉等学者对近10年我国缺血性肠病误诊病例进行荟萃,发现该病误诊率高达63.4%。目前对该病尚无统一的诊断标准,需要综合高危因素、临床表现及辅助检查进行诊断。
肾病综合征与缺血性肠病肾病综合征合并缺血性肠病多为个案报告,一方面与缺血性肠病发病率低有关,另一方面也与对该病的认识不足,导致误诊漏诊有关。国内王军等于2012年报告一例微小病变性肾病合并肠系膜静脉血栓形成患者,消化道症状表现为腹胀、腹泻、恶心、呕吐,增强CT扫描显示脾静脉、肠系膜上静脉、门静脉分支及主干血栓形成,经抗凝、抗血小板治疗后复查血栓明显减少,肾病综合征缓解后消化道症状也明显好转。本例患者,反复于肾病综合征复发后出现消化道症状,伴下消化道出血,消化道临床表现亦能在抗凝、对症治疗后迅速缓解,行消化内镜检查未发现明确肠道病变,排除其他消化道疾病后考虑缺血性肠病可能性大。但遗憾的是,我们虽然对患者进行多项相关检查,除发现部分肠道供血血管稍狭窄之外,未找到明确肠系膜血管内血栓及肠壁黏膜病变。
治疗及预后缺血性肠病根据患者病因不同、临床表现不同而采取不同的治疗方法,其预后也不同。AMI多起病急、病情凶险、死亡率高,常需要行手术治疗,预后与早期诊断和手术重建血运的时间有关。CMI可首先采用内科对症保守治疗,对内科治疗无效患者可采用手术行血管重建术等,多数患者呈长期慢性病程。IC相对预后较好,多数患者具有自限性,且经内科对症治疗效果佳,多不需要手术治疗,对少数合并腹膜炎或中毒性休克患者需早期诊断,积极治疗,降低病死率。