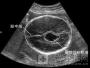
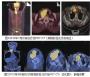
一名有下肢水肿、血尿和急性肾衰竭的77岁男性
2012-07-12 20:57:41 来源:37度医学网 作者: 评论:0 点击:
急进性肾小球肾炎
急进性肾小球肾炎由3种主要类型的疾病导致:抗GBM病(大约10%的病例)、少免疫性新月体性肾小球肾炎(大约60%)以及免疫复合物肾小球肾炎(大约 30%)。当进行评估时,临床医师需要判定经验性免疫抑制治疗的危险和益处。因为尿液分析结果和沉积物中存在变形红细胞,因此我们的患者接受了糖皮质激素 经验性治疗。
肺出血-肾炎综合征[古德帕斯丘(Goodpasture)综合征]
该患者有间歇性咯血史,并且是一名吸烟者。欧内斯特·古德帕斯丘于1918年描述了2例伴有系统性血管炎的肺出血病例,他将这2例病例归因于流感流行3。 后来,肺出血-肾炎综合征被显示是由GBM Ⅳ型胶原的非胶原1(NC1)结构域的自身抗体导致4,5。肺出血-肾炎综合征(也称为抗GBM病)患者往往表现为突然发生的少尿、血尿和急性肾衰竭 6(正如该患者表现的那样)。年龄分布呈双峰——吸烟的年轻男性表现为肺-肾综合征,五六十岁的女性则表现为局限于肾脏的疾病7。吸烟患者(例如该患者) 出现肺受累,可能是因为肺损伤和新表位暴露于免疫系统。通过检测血中的抗体和活检时沉积于GBM的IgG而做出诊断。
根据急性肾小球肾炎和咯血史,该患者可能有抗GBM病。然而,抗GBM抗体检测阴性。
少免疫性(pauci-immune)肾小球肾炎
急进性肾小球肾炎较常见的原因为少免疫性坏死性肾小球肾炎,包括ANCA相关性血管炎(显微镜下多血管炎)、肉芽肿病伴多血管炎[以前的韦格纳肉芽肿 病)]和变应性肉芽肿性血管炎[许尔-施特劳斯(Churg-Strauss)综合征]。显微镜下多血管炎是一种小血管和中血管的血管炎8,通常表现为持 久的全身症状9,80%的患者肾脏受累10,20%~55%的患者肺受累11。多发性单神经炎和皮肤病变较少发生12。患者表现为血尿,有或没有蛋白尿, 偶尔在肾病范围内,10%~46%的患者需要透析9,10,12。在50%~75%的患者中可见针对髓过氧化物酶的循环ANCA(p- ANCA)10,13,14。在活动性肾病患者中,检测ANCA以诊断显微镜下多血管炎的阳性预测值范围为47%~99%15。
肉芽肿病伴多血管炎通常累及上和下呼吸道,并且与肾小球肾炎相关。在发生系统性血管炎之前,该病可呈惰性,累及鼻窦(慢性鼻窦炎)、耳(中耳炎)和气管 (气管狭窄)16。该病主要累及40多岁的白人男性和女性17,18。大多数患者有上气道或肺受累,表现不一,可为空洞形成结节至弥漫性肺泡出血。
1/3~1/2的患者出现眼部疾病。皮肤受累可包括血管炎性皮疹和非愈合性溃疡。该患者有咯血和皮疹,但没有上气道疾病。大多数患者针对蛋白酶3的 ANCA(c-ANCA)检测阳性,免疫荧光染色呈胞质分布19。ANCA检测敏感性达90%,特异性达98%。在该病例,ANCA检测阴性不支持肉芽肿 病伴多血管炎的诊断,但也无法排除该诊断。
第3种ANCA相关性疾病是变应性肉芽肿性血管炎,特征为哮喘、嗜酸粒细胞增多、肉芽肿性血管炎和组织嗜酸粒细胞浸润20-22。该病发生于30多岁和 40多岁的患者(与该患者不符),男性 (患者)稍多。肾脏受累通常为轻度,这与该病例不符23。在65%的患者中可检出针对髓过氧化物酶的ANCA(p-ANCA)。嗜酸粒细胞增多和IgE水 平升高为特征性表现。我们的患者没有任何哮喘或嗜酸粒细胞增多,这使变应性肉芽肿性血管炎不太可能。
免疫复合物肾小球肾炎
需要考虑的免疫复合物肾小球肾炎包括低补体血性组和正常补体血性组。与低C3水平相关的病症包括系统性红斑狼疮、链球菌感染后肾小球肾炎、膜增生性肾小球 肾炎、心内膜炎、内脏脓肿和分流性肾炎。与低C4水平相关的主要病症为冷球蛋白血症。正常补体血性肾小球肾炎主要包括IgA肾病、过敏性紫癜[亨诺克-舍 恩莱因(Henoch-Schönlein)紫癜]和纤维性肾小球肾炎。
感染后肾小球肾炎发生于上呼吸道感染或皮肤感染后24,25。没有可解释该患者疾病的前驱感染。心内膜炎导致的免疫复合物肾小球肾炎在前抗生素时代比在目 前常见得多26-29。我们见过细菌(包括金黄色葡萄球菌)感染触发的过敏性紫癜病例30。在该患者,没有感染或脓毒症的证据。
3种类型冷球蛋白血症中的任何1种(Ⅰ型,单克隆型;Ⅱ型,单克隆加多克隆型;Ⅲ型,多克隆型)31均累及皮肤,伴有瘀点性皮疹、网状青斑、溃疡和指 (趾)缺血。其他表现包括关节炎、中枢神经系统受累、心脏受累、胃肠血管炎和肺受累。该患者有皮疹和肾病,这提高了冷球蛋白血症的可能性。然而,他没有感 染(例如丙型肝炎)或通常伴有冷球蛋白血症的克隆型或恶性血液学病症的危险因素和临床表现32,33。
系统性红斑狼疮最常见于年轻女性,但也可发生于老年人和男性。表现包括皮肤、关节、浆膜、胃肠、肾脏、精神、肺以及血液学表现。狼疮肾炎患者的症状可从无(症状)至急进性肾小球肾炎。这名老年男性患者没有系统性红斑狼疮的典型特征。
IgA肾病和过敏性紫癜是导致肾小球肾炎的IgA沉积疾病。IgA肾病34是肾小球肾炎最常见的原因,症状(范围)从无症状的血尿至急进性肾小球肾炎 35。蛋白尿、高血压、老龄、男性、黑色人种以及肾活检标本检查时存在瘢痕和新月体均与IgA肾病患者预后差相关36。过敏性紫癜和肾病患者有可触及的紫 癜和胃肠表现(包括腹痛、出血、梗死和肠套叠)37。该患者有急进性肾小球肾炎和皮疹,可能存在IgA介导的(疾病)过程。然而,肾活检标本未显示IgA 沉积。
小结
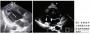
在1例急进性肾衰竭患者中,发现红细胞管型允许临床上分类为急进性肾小球肾炎。我们可进行序贯血清学评估(图2),但器官受累模式可能有助于确定某种疾病 的预测概率(表2)。抗GBM抗体有高度敏感性和特异性,并且它们的存在可通过蛋白质印迹分析所证实。相似地,临床综合征典型时可诊断ANCA相关性血管 炎,而证实性组织诊断可能并非必要。在该患者,血清学评估阴性,但肾活检标本的检查结果被解释为抗GBM病。

面对阴性血清学测定和显示抗GBM病的活检标本,我们不得不探讨该检测的局限性,并考虑结果是否有可能为假阴性。酶联免疫吸附测定(ELISA)结果有可 能为假阴性,或者活检标本有可能显示IgG(而非真正的抗GBM抗体)的非特异性结合。此外,即使一项检测的敏感性为98%,仍有2%的抗GBM病患者 (检测)阴性。我们考虑了如下可能性:该患者的抗体主要以高亲和力结合至肾脏,仅以低于ELISA敏感性的低水平进行循环38。有研究显示,亲合力较高的 抗体与较严重的疾病相关39。另一种可能性是抗GBM抗体的靶抗原不是NC1。在家族性出血性肾炎[奥尔波特(Alport)综合征]患者(有Ⅳ型胶原基 因突变)中,移植后有可能发生抗GBM病,作为对同种异基因移植物的正常抗原的反应。还有一篇关于抗GBM病的抗原为一种肾脏59-kD抗原的病例报告 40。应通过蛋白质印迹分析检测这些新的自身抗体,用这种方法筛查该患者血清中针对古德帕斯丘抗原的自身抗体。

基于上述临床表现,我们认为该患者有导致抗GBM病的低滴度、高亲和力抗体。因此,我们要求进行蛋白质印迹分析,以寻找该患者血清中结合27-kD和 54-kD蛋白(出现于GBM的胶原酶消化时,在Ⅳ型胶原α3链的NC1结构域中形成单体和二聚体)的一种抗体41,42。如果抗IgG2和抗IgG3免 疫荧光产生的染色比传统IgG1染色明显,我们还可寻求亚类分析。
埃里克·S·罗森堡医师(病理科):赖斯曼医师,你能告诉我们当该患者到达(医院)时你和你的团队是如何考虑的吗?
赖斯曼医师:当该患者于凌晨1点到达时,我们知道他有急进性肾衰竭,活检检查显示新月体性肾小球肾炎证实了这点。鉴别诊断包括ANCA相关性血管炎、抗 GBM病、狼疮、链球菌感染后肾小球肾炎、过敏性紫癜和IgA肾病。该患者的一次咯血发作史提示肺出血-肾炎综合征,呕吐则提示伴有胃肠受累的过敏性紫 癜。检查时,他下肢的皮疹不可触及。然而,他肯定地说1或2周前如果他闭眼用手抚过皮疹,他可感觉到皮疹的质地。我们(当时)在等待血清学检测结果,并且 尿样本的显微镜检查显示蛋白尿、血尿和大量颗粒管型。该患者已接受糖皮质激素治疗以阻止肾功能下降。第一晚较直接的担心包括(如何)控制他的高血压,尤其 是考虑到他有增大的腹主动脉瘤。
哈桑·巴扎里医师的诊断
肺出血-肾炎综合征。
病理讨论
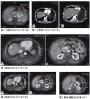
耶尔·B·库什纳医师:(该患者)在另一家医院进行了肾活检,并且标本被送来(本院)检查。福尔马林固定组织的光学显微镜检查显示肾小囊腔 (urinary space)内的肾小球伴有大量细胞性和纤维细胞性新月体(图3A)。下层肾小球有增生外观,偶有发育良好的系膜结节形成(图3B)。一些肾小球有系膜细 胞核的丢失以及系膜基质呈花边样、被破坏的外观(称为系膜溶解)(图3C)。其他肾小球显示节段性或整体性硬化,并且黏附于肾小囊。过碘酸-希夫染色可见 局灶性重复的GBM。有轻微间质炎性浸润。我们在肾小管间质间隔中还辨别出间质纤维化和肾小管萎缩的慢性改变。肾小管显示轻度急性损伤,伴有上皮细胞空泡 形成和再生性改变。一些小动脉显示水肿明显,伴有局灶性管腔闭塞和壁内破碎的红细胞。小动脉含有一些壁内透明变性。

对冰冻组织进行的免疫荧光检查(图3D)显示沿GBM呈线性模式的相对强IgG染色。细胞新月体内可见纤维蛋白。节段性瘢痕肾小球内可见IgM和C3。电 子显微镜显示足细胞足突广泛消失[(图)未显示]。此外,内皮细胞显著水肿,伴有局灶性内皮下电子透明物质。未见沉积物,并且没有管网状包涵体或免疫复合 物肾小球肾炎或自身免疫病的其他征像。
肾活检标本检查所见的细胞新月体等同于急进性肾小球肾炎临床综合征的病理(表现)。根据免疫荧光模式可区分抗GBM病、少免疫性(ANCA相关性)肾小球 肾炎和免疫复合物肾小球肾炎。在该病例,沿GBM有线性IgG免疫荧光反应对抗GBM病具有诊断性,同时有肺部表现则被称为肺出血-肾炎综合征。在该患 者,尽管最初抗GBM抗体的ELISA阴性,但之后用蛋白质印迹分析检出了抗GBM抗体(图3E)。
存在明显的结节性肾小球改变提高了糖尿病肾病的可能性,这有可能是该病例一处重要的陷阱,因为来自糖尿病患者组织标本的免疫荧光检查也可显示线性IgG模 式,而该患者最初的抗GBM抗体检测阴性。然而,该患者没有糖尿病。结节性肾小球硬化存在其他可能性吗?根据免疫荧光和超微结构的(检查)结果以及临床病 史可排除副蛋白质沉积和膜增生模式的免疫复合物疾病(例如膜增生性肾小球肾炎和冷球蛋白血症)。有人描述了一种称为特发性结节性肾小球硬化的疾病,该病通 常见于有高血压和吸烟的中年男性43。存在系膜溶解的情况下该诊断是可能的,因为系膜溶解愈合后有可能变成结节模式。
小动脉水肿、管腔闭塞伴壁内破碎红细胞的存在以及内皮损伤的超微结构征象均提示亚临床血栓性微血管病。典型原因包括恶性高血压、抗磷脂抗体综合征[由狼疮 抗凝物或其他抗磷脂(抗体)(例如抗心磷脂抗体或抗B2-糖蛋白1抗体)检测阳性提示]、硬皮病、溶血尿毒综合征或血栓性血小板减少性紫癜以及有血管毒性 效应的药物。然而,在该病例,导致系膜溶解和结节性肾小球硬化的相同损伤(吸烟和高血压所致)也有可能导致小动脉内皮损伤。
巴扎里医师:证实有抗GBM病的患者接受糖皮质激素、环磷酰胺和血浆置换治疗44。积极治疗可提高患者生存率(接近85%)。治疗后的肾脏生存率为 65%,预后差的标准为发病时少尿和血清肌酐水平>6 mg/dl(530.4 μmol/L)45。血浆置换持续至不再检出抗体。
罗森堡医师:赖斯曼医师,你能否告诉我们该患者怎么样了?
赖斯曼医师:我们持续(给予)糖皮质激素治疗,用血浆置换清除抗GBM抗体,并且开始给予环磷酰胺治疗。因为(我们)担心(动脉瘤)破裂,所以该患者在住 院第10天进行了开腹主动脉瘤修复术。出院时(第21天),他的血清抗GBM抗体水平已无法检出,他的肌酐水平为3 mg/dl(265 μmol/L)。2周后,他出现了需要血液透析的进行性肾衰竭。此后1个月,(他)发生了内脏穿孔,并且(医师)确定外科修复术不在他的治疗目标内。此后 不久,该患者死亡。
罗森堡医师:有什么问题吗?
劳埃德·阿克塞尔罗德医师(内分泌科):巴扎里医师,我对你关于微血管病组成的看法感到很好奇,该结果的根据是什么?
巴扎里医师:该患者没有微血管病性溶血性贫血。他有肾脏血栓性微血管病的证据,但并不一定是全身性血栓性微血管病。活检标本存在的血栓性微血管病(没有微血管病性溶血性贫血的结果)由局部因素导致的可能性最大,并且不是全身疾病的表现。
一名内科医师:在没有导致他死亡的共存病况的情况下,肾病的自然史是怎样的?
巴扎里医师:该患者有4期慢性肾病,肌酐水平>3 mg/dl。抗GBM病倾向于自限,我们通常治疗3~6个月,或直至抗GBM抗体滴度无法检出。如果存在终末期肾病,我们仍会注意(抗体)滴度,因为肺出血可伴随着抗GBM病复发而发生。
解剖学诊断
肺出血-肾炎综合征。
(N Engl J Med 2012;366:2503-15.June 28,2012) [1050101]
上一篇:子宫外产时处理的临床应用
下一篇:早期手术与常规治疗对感染性心内膜炎的疗效比较
论坛新帖
频道总排行
医学推广
频道本月排行
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(11)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)