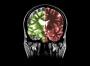
解释癫痫中的耐药性
2013-07-31 10:46:30 来源:37度医学网 作者: 评论:0 点击:
研究人员表示,脑部某些部位中 P-糖蛋白过度活化与抗癫痫药物耐药性有关
背景
癫痫的啮齿类动物模型研究表明,血脑屏障中的多药转运蛋白(如 P-糖蛋白)可能通过降低靶位点的抗癫痫药物浓度而引起耐药性。 我们在颞叶癫痫患者中对 P-糖蛋白在其体内的活性进行了评估。
方法
我们选择了 16 名已接受了至少两种抗癫痫药物,但仍出现癫痫发作的耐药性颞叶癫痫患者,八名至少具有 3 年活动性颞叶癫痫病史,但在抗癫痫药物治疗后至少一年未发生癫痫的患者,以及 17 名健康对照者。 所有参与者均接受了 P-糖蛋白底物 (R)-[11C] 维拉帕米基线 PET 扫描。 接着,耐药性患者和健康对照者均接受了 30 分钟的 P-糖蛋白抑制剂他立喹达 (tariquidar) 输注,并在 60 分钟后再次接受了 (R)-[11C] 维拉帕米 PET 扫描。 无癫痫发作的患者在同一天接受了第二次扫描,但未接受他立喹达输注。 我们利用体素计算了 (R)-[11C] 维拉帕米的血浆至脑内转运速率常数,K1 (mL/min/cm3)。 较低的基线 K1 和输注他立喹达后 K1 增幅减小对应于较高的 P-糖蛋白活性。
结果
在 2008 年 10 月至 2011 年 11 月之间,我们在 14 名耐药性患者、八名无癫痫发作患者和 13 名健康对照者中完成了 (R)-[11C] 维拉帕米 PET 研究。 基于体素的分析表明,与无癫痫发作的患者相比,在同侧杏仁核 (0·031 vs 0·036 mL/min/cm3; p=0·014)、双侧海马旁回 (0·032 vs 0·037; p<0·0001)、梭状回 (0·036 vs 0·041; p<0·0001)、颞下回 (0·035 vs 0·041; p<0·0001) 和颞中回 (0·038 vs 0·044; p<0·0001) 中,耐药性患者的基线 K1 较低时,则对应于较高的基线 P-糖蛋白活性。 较高的 P-糖蛋白活性与全脑灰质 (p=0·016) 和海马 (p=0·029) 中较高的癫痫发作频率相关。 我们发现,健康对照者在接受 2 mg/kg 的他立喹达后,全脑 K1 增大了 56·8%,在剂量为 3 mg/kg 时则增大了 57·9%;而耐药性颞叶癫痫患者在接受剂量为 2 mg/kg 他立喹达时,全脑 K1 仅增大了 21·9%,在剂量为 3 mg/kg 时则增大了 42·6%。 他立喹达应答的差异在硬化型海马中最为明显(在患者中平均增大 24·5%;在健康对照者中平均增大 65%,p<0·0001)。
结果解读
我们的研究结果支持这一假说,即脑部某些区域中的 P-糖蛋白过度活化与颞叶癫痫的耐药性相关。 如果该关系得到确认,我们便可确定 P-糖蛋白为耐药性的一个因素,只要我们能够克服 P-糖蛋白过度活化,便可将其作为潜在的治疗策略加以研究。
Feldmann M, Asselin MC, Liu J, et al. P-glycoprotein expression and function in patients with temporal lobe epilepsy: a case-control study. Lancet Neurol. 2013;12:777-85.
背景
癫痫的啮齿类动物模型研究表明,血脑屏障中的多药转运蛋白(如 P-糖蛋白)可能通过降低靶位点的抗癫痫药物浓度而引起耐药性。 我们在颞叶癫痫患者中对 P-糖蛋白在其体内的活性进行了评估。
方法
我们选择了 16 名已接受了至少两种抗癫痫药物,但仍出现癫痫发作的耐药性颞叶癫痫患者,八名至少具有 3 年活动性颞叶癫痫病史,但在抗癫痫药物治疗后至少一年未发生癫痫的患者,以及 17 名健康对照者。 所有参与者均接受了 P-糖蛋白底物 (R)-[11C] 维拉帕米基线 PET 扫描。 接着,耐药性患者和健康对照者均接受了 30 分钟的 P-糖蛋白抑制剂他立喹达 (tariquidar) 输注,并在 60 分钟后再次接受了 (R)-[11C] 维拉帕米 PET 扫描。 无癫痫发作的患者在同一天接受了第二次扫描,但未接受他立喹达输注。 我们利用体素计算了 (R)-[11C] 维拉帕米的血浆至脑内转运速率常数,K1 (mL/min/cm3)。 较低的基线 K1 和输注他立喹达后 K1 增幅减小对应于较高的 P-糖蛋白活性。
结果
在 2008 年 10 月至 2011 年 11 月之间,我们在 14 名耐药性患者、八名无癫痫发作患者和 13 名健康对照者中完成了 (R)-[11C] 维拉帕米 PET 研究。 基于体素的分析表明,与无癫痫发作的患者相比,在同侧杏仁核 (0·031 vs 0·036 mL/min/cm3; p=0·014)、双侧海马旁回 (0·032 vs 0·037; p<0·0001)、梭状回 (0·036 vs 0·041; p<0·0001)、颞下回 (0·035 vs 0·041; p<0·0001) 和颞中回 (0·038 vs 0·044; p<0·0001) 中,耐药性患者的基线 K1 较低时,则对应于较高的基线 P-糖蛋白活性。 较高的 P-糖蛋白活性与全脑灰质 (p=0·016) 和海马 (p=0·029) 中较高的癫痫发作频率相关。 我们发现,健康对照者在接受 2 mg/kg 的他立喹达后,全脑 K1 增大了 56·8%,在剂量为 3 mg/kg 时则增大了 57·9%;而耐药性颞叶癫痫患者在接受剂量为 2 mg/kg 他立喹达时,全脑 K1 仅增大了 21·9%,在剂量为 3 mg/kg 时则增大了 42·6%。 他立喹达应答的差异在硬化型海马中最为明显(在患者中平均增大 24·5%;在健康对照者中平均增大 65%,p<0·0001)。
结果解读
我们的研究结果支持这一假说,即脑部某些区域中的 P-糖蛋白过度活化与颞叶癫痫的耐药性相关。 如果该关系得到确认,我们便可确定 P-糖蛋白为耐药性的一个因素,只要我们能够克服 P-糖蛋白过度活化,便可将其作为潜在的治疗策略加以研究。
Feldmann M, Asselin MC, Liu J, et al. P-glycoprotein expression and function in patients with temporal lobe epilepsy: a case-control study. Lancet Neurol. 2013;12:777-85.
上一篇:癫痫中的精神并发症
下一篇:阿尔兹海默病生物标志物在额颞部痴呆诊断中具有局限性
论坛新帖
频道总排行
医学推广
频道本月排行
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(11)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)