三阴性乳腺癌:探索与进展
2012-04-12 16:12:35 来源:医学论坛网 作者: 评论:0 点击:
三阴性乳腺癌(TNBC)是指雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)表达均为阴性的乳腺癌。随着研究的深入与细化,基于分子生物学因素对肿瘤进 行个体化治疗成为今后的趋势,即通过检测分子生物学标志物,预测患者对某种治疗的反应和预后,从而选择出优势人群,给予更具针对性的治疗,以取得 最大 的获益、最小的不良反应。TNBC患者无法接受针对ER和PR的内分泌治疗及针对HER2的分子靶向治疗,目前有效的全身治疗措施只有化疗。因此,寻找能 够影响或预测TNBC 疗效、预后的分子生物学因素,具有重要的临床意义。
已有的研究显示,TNBC患者肿瘤体积较大,病理类型多为导管癌,组织学分级较高,肿瘤细胞多表达基底细胞角蛋白(CK5/6、CKl7)、 P-cadherin、EGFR 和p53,较少表达雄激素受体(AR)、E-钙黏素和细胞同期素D。但针对TNBC 的分子表达谱目前尚未见报道,对这 一特殊类型乳腺癌的认识多从基底样乳腺癌和BRCA1相关乳腺癌的研究中获得。
AR
AR是核受体,依赖雄激素调节相关基因参与细胞的增殖和分化。Ortrnann等在体外试验中发现,雄激素对AR高表达乳腺癌细胞系的生长具有抑制作用。AR 在乳腺癌中的作用尚不清楚,通常认为其表达对乳腺癌具有保护作用。
Rakha等检测了1726例浸润性乳腺癌患者的激素受体和HER2表达情况,在282例三阴性表型中,234 例(87%)丢失了AR的表 达。AR 表达缺失与高组织学分级(P <0.001),复发(P =0.038)及远处转移相关(P =0.049),提示AR 表达缺失可能与恶性表 型和肿瘤侵袭进展有关。在全部TNBC中,AR与肿瘤大小、淋巴结状态是同等重要的预后指标。在淋巴结阳性亚组中,AR 和肿瘤大小能够预测预后。因此, 在常用病理检测中明确是否存在AR表达及基底样表型,对手术后区分低危与高危患者,予以不同的治疗有着重要意义。
P53
P53是迄今为止被发现与人类肿瘤相关性最高的基因,几乎>50%的癌症都与p53有关。P53分为野生型和突变型两种。野生型p53是一种抑 癌基因,可以阻滞癌细 胞周期、诱导癌细胞凋亡和促进癌细胞分化;突变型p53则丧失了抑癌作用,成为一种肿瘤促进因子,具有促进肿瘤形成、转化细胞活性 的作用。P53突变的乳腺癌侵袭 性强、转移率高、放疗不敏感且易对化疗药物产生耐受,患者预后较差。
国外有文献报道,TNBC中P53蛋白的阳性表达率较高,国内报道的P53蛋白阳性表达率约为52.38%,并且与患者的年龄、肿瘤大小、淋巴 结转移、月经状态没有明显相关性(P >0.05)。但P53 蛋白表达对于TNBC预后影响的研究报道存在不一致的结论。一项有较长随访时间的大样本 TNBC分析研究表明,P53蛋白的表达与病理组织学分级高相关。多因素分析显示,仅肿瘤大小是独立的预后指标,P53蛋白与患者预后无关。
Chae分析了135例接受含蒽环类药物方案进行辅助化疗的乳腺浸润性导管癌患者资料后发现,全部患者中有57例(42.2%)为P53 蛋白 阳性,TNBC 患者中13 例(40.6%)为P53蛋白过表达,非三阴性患者中44例(42.7%)为过表达。在全部患者和非三阴性患者中没有观察到 p53状态对总生存和无复发生存的影响,但在TNBC 组 中,P53蛋白阳性患者的总生存以及无复发生存均明显差于P53蛋白阴性者 (P =0.034,P =0.005)。单因素分析显示,p53 状态与TNBC 患者的总生存和无复发生存相关。多因素分析显示,p53状态是 TNBC患者无复发生存的独立影响因素(P =0.013)。这提示P53 蛋白可用作TNBC 患者接受蒽环类药物方案治疗的独立预后指标。
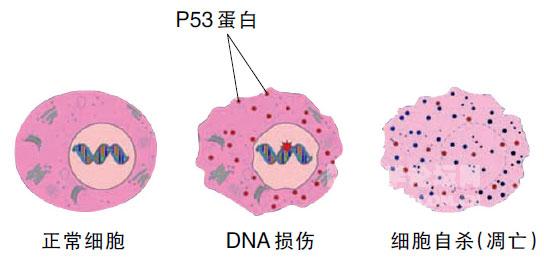
图P53 肿瘤抑制蛋白启动细胞自杀
BRCA1 及DNA修复通路
BRCA1是一个重要的抑癌基因,其结构和功能的异常与乳腺癌的发病密切相关。TNBC 中BRCA1 基因的突变率高,多数TNBC 存在 BRCA1 缺陷、BRCA1 表达下降或缺失。BRCA1的缺失不仅可以直接导致基因组的异常,还可以导致损伤DNA修复障碍、中心粒的扩增以及重要细 胞检测点的异常,从而造成BRCA1突变细胞的遗传不稳定。
与不携带BRCA1突变的乳腺癌患者相比,BRCA1 相关性乳腺癌组织分化差、ER和PR 常呈阴性,提示预后可能较差。Kar等发 现,BRCA1突变者的腋窝淋巴结转移率高,而Armes、Robinsin和Eisinger等的研究却没有发现上述差异。BRCA1能否作为一个独立 的预后指标仍有争议。
研究发现,BRCA1表达水平低的患者对铂类药物敏感,表达水平高的患者则表现为对铂类药物耐药。抗微血管药物,如紫杉醇、多西他赛、长春新碱和长春瑞滨等的疗效也与肿瘤组织中BRCA1的mRNA表达水平密切相关。BRCA1表达水平高的患者对抗微血管药物敏感,表达水平低者则对其耐药。
切除修复交叉互补基因l(ERCCl)是损伤DNA修复系统中的一个关键基因。所有肿瘤细胞中都有ERCC1表达,但表达水平差异较大。大约 1/4~1/3 的TNBC 患者有一定程度的ERCC1 表达。Sidoni 在81 例100%不表达ER、PR、HER2 的乳腺癌中检测 ERCC1的表达情况,发现ERCC1的表达与其他主要临床病理影响因素不相关。与非小细胞肺癌一样,乳腺癌中ERCC1的表达也与顺铂耐药有 关,ERCC1表达水平低者对铂类药物敏感,以铂类药物为基础的化疗方案可能对这部分患者有较好的疗效。在对TNBC患者予以含铂方案治疗时可以先检测其 肿瘤组织的ERCCl表达状况以预测疗效。
表皮生长因子受体及其信号通路
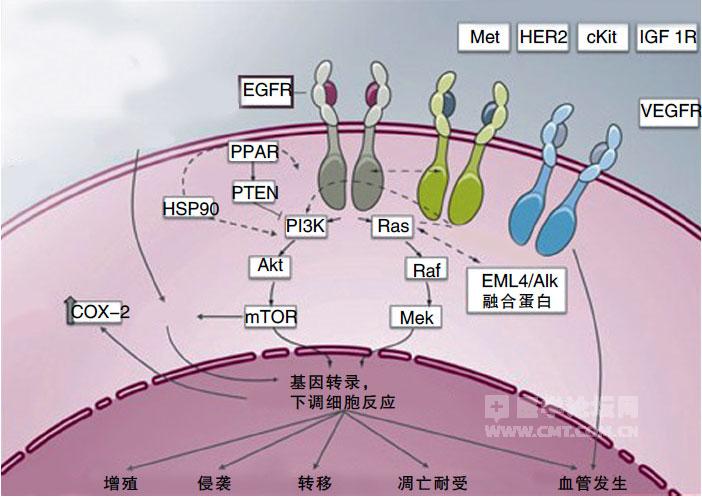
图EGFR 信号传导通路
EGFR在TNBC中表达率约为60%,其信号传导通路往往与TNBC的发生发展密切相关。越来越多的研究关注与EGFR及其信号传导通路有关的靶向治疗。本文对近年来EGFR 信号传导通路与TNBC 发生发展的关系以及针对该传导通路的靶向治疗研究进展作一综述。
EGFR在包括TNBC在内的多种人类恶性实体瘤中存在过表达或突变,并通过介导多种途径的信号通路调控细胞的生长、分化、增殖、迁移和存活等,常与预后不良、转移快、短期复发、生存期短等相关。因此EGFR及其下游信号传导通路已成为TNBC治疗研究的重要靶点。
EGFR与相应的配体结合活化,引起受体的同源或异源二聚体化,导致受体胞内区酪氨酸激酶区激活,使二聚体内特异的酪氨酸残基发生自身磷酸化, 从而激活众多的下游信号通路。其中最主要的信号传导通路包括Ras/Raf/MEK/ERK信号通路和磷脂酰肌醇3-激酶(PI3K)/蛋白激酶B(又称 Akt)信号通路。EGFR 又称为HER1 或ErbB-1。日本研究者进行了一项关于EGFR表达与乳腺癌疗效及预后关系的回顾性研究,发现EGFR 阳性表达在激素受体阳性亚型中提示临床治疗反应较好(P =0.06),生存期较长(P =0.11),而在三阴性亚型中却与化疗应答不佳 (P =0.03)、预后较差(P =0.17)相关。
EGFR信号通路与TNBC的发生发展许多研究表明,EGFR高表达在大多数TNBC的发生发展中起重要作用。Corkery等的研究证实了上 述发现,他们认为与HER2阳性细胞系比较,TNBC中存在EGFR的更高表达,并且表皮生长因子(EGF)作用后可看到TNBC 细胞系中EGFR 的 磷酸化。而EGFR 的磷酸化可导致包括MEK/ERK和PI3K/Akt通路在内的下游信号传导通路的激活,引起相关基因的转录表达,从而抑制肿瘤细胞 的凋亡,促进肿瘤细胞的生长、增殖、转移及血管的生成,进而促进肿瘤的发展。
EGFR信号通路是个非常复杂的网络,其中各种成分的基因表达水平在不同乳腺癌亚型中有所不同。三阴性/基底样乳腺癌亚型与EGFR-RAS- MEK 通路中的许多基因如EGFR、人转化生长因子-α(TGF-α)、MEK1、MEK2、Akt3 等的高表达显著相关。而与TNBC的活化信号通 路相关的几个基因,包括有丝分裂原活化蛋白激酶/细胞外 信号调节激酶(MAPK-ERK)、PI3K-Akt、P38 激酶和NF-κB 在肿瘤中也 比较常见。这些下游信号通路如PI3K-Akt 通路、MAPK-ERK通路及NF-κB的活化在TNBC的发生发展中可能起到了关键作用,并可能作为 TNBC治疗的靶点。
Umemura 等发现,TNBC 中ERK1/2 的磷酸化水平略高于其他组;而Akt激酶的磷酸化水平显著高于其他组。因此,他们认 为,Akt激酶的磷酸化水平增加是TNBC的特点,并且第一次在这种乳腺癌亚型中发现Akt通路的明显活化。其他研究者通过对TNBC肿瘤中表达的几个受 体如EGFR、胰岛素样生长因子1 受体(IGF1R)、HER3和c-Kit 证实,肿瘤可通过Ras/Raf/MEK/ERK 通路的活化来增加增殖 潜力。Oliveras-Ferraros 等在三阴性/基底样乳腺癌MDA-MB-468 细胞株的研究中也发现了这一现象,他们不仅检测到了 EGFR 的过表达,而且还有EFGR 细胞内下游信号通路的活化(例如MEK/ERK 通路和PI3K/Akt通路)。
因此,EGFR 及其信号传导通路与TNBC的发生发展密切相关。该通路的异常活化能导致肿瘤细胞的增殖、存活等,促进肿瘤的发展。因此阻断该信号通路的传导对于TNBC的治疗具有重大的意义。
EGFR信号通路与TNBC的靶向治疗
针对EGFR的分子靶向药物通过不同途径阻断EGFR介导的细胞内信号通路,从而抑制肿瘤生 长、转移和血管生成,并促进肿瘤细胞凋亡。目前主要有两类药物:一类是抑制EGFR胞内区酪氨酸激酶活性的小分子酪氨酸激酶抑制药(TKI),如吉非替尼 和厄洛替尼;另一类是与EGFR胞外区结合,阻断配体依赖的EGFR活化的单克隆抗体(mAb),如西妥昔单抗和帕尼单抗。
由于TNBC细胞多表达EGFR,很多学者致力于EGFR 的单克隆抗体及TKI 在TNBC 中的研究。尽管研究显示,EGFRTKI如吉非 替尼等的耐药现象在乳腺癌中较常见,然而Corkery 等通过体外试验发现,吉非替尼增强了卡铂和多西他赛在TNBC细胞中的作用,三者在TNBC中是 协同作用。TNBC 细胞系对于EGFR 抑制药的反应与MAPK和Akt磷酸化的减少和诱导G1期的阻滞有关。Thome报道一项使用吉西他滨加厄洛替 尼治疗转移性乳腺癌的Ⅱ期临床研究。共57例可评价病例,TNBC为20 例,部分缓解(PR)率达25%,而非TNBC中PR率仅为14%。
西妥昔单抗单药治疗TNBC曾显示出一定疗效。而Carey等研究发现,相对于西妥昔单抗单药,西妥昔单抗联合卡铂可能对TNBC 的疗效更好 (有效率为6% 对17%),但这一差别并没有统计学意义。然而,体外试验发现,MDA-MB-468细胞株中西妥昔单抗和最佳剂量顺铂的同时使用可使 EGFR蛋白完全耗尽。这一结果提示,我们在联合使用抗EGFR抗体和铂类药物治疗三阴性/基底样乳腺癌时应该仔细考虑治疗的时间安排、西妥昔单抗/顺铂 的剂量及BRCA 1的状态,以达到更好的治疗效果。在西妥昔单抗联合伊立替康和卡铂治疗72例TNBC的亚组分析中,西妥昔单抗增加了客观缓解率 (ORR,13%~19%),但这一改善并没有带来无进展生存(PFS)期的延长。最近,Nechushtan等在2009年ASCO会议上报道了西妥昔 单抗联合紫杉类方案治疗12例TNBC患者的Ⅰ/Ⅱ期临床试验结果,紫杉类药物与西妥昔单抗每周方案的有率较高(81.8%),耐受性也较好。
前期试验证实Src 抑制药达沙替尼(dasatinib)能够抑制肿瘤细胞增殖和转移活性,且基因表达谱显示Basal-like型乳腺癌可 能对达沙替尼治疗敏感。Finn 等报道了采用达沙替尼治疗进展期TNBC的Ⅱ期临床试验结果,发现达沙替尼具有抗TNBC 的活性,单药有效率为 9.3% 。Nautiyal 等通过体外试验发现,达沙替尼可通过调节EGFR 信号来抑制包括TNBC在内的乳腺癌细胞的生长。达沙替尼在TNBC中 的具体作用机制及临床应用的剂量、疗程及化疗联合应用方面的研究还有待进一步开展。
另外,还有一些其他药物在体内外实验中显示出与EGFR信号传导通路有关的抗TNBC 作用。Phoenix 等研究发现,二甲双胍在MDA- MB-231 细胞株中主要通过降低MAPK1/2 磷酸化水平而抑制细胞增殖。Bolin等进一步研究发现二甲双胍在体内和体外均有着独特的抗 TNBC 的作用。它可以通过激活仅存在于TNBC细胞系中的内源性和外源性信号通路来抑制细胞的增殖(部分S 期阻滞)、克隆形成并诱导凋亡。在分子水 平,二甲双胍减少了TNBC细胞中细胞周期蛋白的水平并使EGFR及下游信号失活,而对其他亚型的乳腺癌细胞没有这种作用。最近,研究者发现HSP90抑 制药PU-H71可在体内外诱导一些蛋白有效而持久的下调和失活,其中包括下调Ras/Raf/MAPK通路及G2-M期的蛋白以利于抗增殖作用,降解分 解活化的Akt 和Bcl-xl 以诱导凋亡,抑制活化的NF-κB、Akt、ERK2、Tyk2和PKC以降低TNBC的侵袭潜力。因此,二甲双胍和 PU-H71 在TNBC中显示出了很好的抗肿瘤作用,具有很好的临床应用前景。
除此之外,瘦素(leptin)因其在TNBC细胞中的表达也受到了广泛关注。既往研究显示,瘦素不仅可以通过激活蛋白酪氨酸激酶(JAK)/ 转录激活因子3(STAT3)、ERK1/2和(或)PI3K通路诱导乳腺癌细胞的生长,而且可以诱导血管内皮生长因子(VEGF)的表达来调节血管生 成。Saxena等进一步研究证实,瘦素和IGF-1 可通过obRb 和IGF1R 协同激活EGFR 并促进TNBC细胞的增殖、侵袭和迁移,而使用 厄洛替尼和拉帕替尼可有效抑制瘦素和IGF-1诱导的侵袭和迁移。而最近Naviglio等在MDA-MB-231细胞株中研究发现,当环磷酸腺苷 (cAMP)水平升高时,瘦素可促使细胞凋亡。因此,以瘦素信号为靶点的干预治疗可能成为治疗TNBC的新方法。
PTEN基因
PTEN 的全称为与细胞骨架蛋白同源的第10号染色体缺失的磷酸酶基因,又称MMACl、TEPl,是目前发现的第一个具有脂质磷酸酶和蛋白磷酸酶双特异活性的抑癌基因。
研究发现,PTEN与肿瘤的发生发展密切相关,在乳腺癌、胃癌、肝癌、前列腺癌等多种肿瘤中存在表达下调或功能缺失,并且其下调或功能缺失的程 度与肿瘤的恶性 情况呈正相关。南方医科大学附属深圳医院采用免疫组化染色法检测57例基底细胞样型浸润性乳腺癌中PTEN 的表达情况,PTEN阳性 表达率为38.6%,而非特殊型浸润性导管癌中PTEN阳性表达率是72.5%,两者差异具有统计学意义(P =0.001)。这表明抑癌基因PTEN的 表达缺失参与了基底细胞样型浸润性乳腺癌的发生和发展。
PTEN 基因还可作为许多肿瘤预后的评价指标。研究发现,PTEN蛋白的表达与一些恶性肿瘤的生物学行为和预后关系密切,PTEN 蛋白阳性 表达的肿瘤一般分化好、生长速度慢、不易发生转移,预后良好。Depowski 等的研究显示,浸润性乳腺癌PTEN蛋白阳性表达率显著低于早期浸润性 癌;有淋巴结转移的乳腺癌组织中PTEN 蛋白阳性表达率显著低于无淋巴结转移乳腺癌。Winter等的研究证实,PTEN是浸润性导管癌的一个生物学预 后指标,PTEN表达越低,肿瘤核分级越高,ER阳性率越低,无复发生存时间越短。Tsutsui 随访研究了236 例乳腺浸润性导管癌,发现PTEN 表达缺失者无病生存期短于PTEN高表达者,预后不良。PTEN在TNBC中的作用与意义尚有待进一步研究。
小结与展望
TNBC 由于其自身独特的临床病理和分子特征得到越来越多的关注,这部分患者除化疗外尚无其他有效的全身治疗措施,并且疗效和预后之间也存有 差异,依靠现有的肿瘤组织学分级、原发肿瘤大小、淋巴结状态、ER、PR、HER2 等指标难以对TNBC 患者进行个体化的治疗和预后分析。 TNBC 中多存在EGFR 的高表达及EGFR信号传导通路的异常活化。这一现象可能与其增殖快、侵袭力强、远处转移风险高和预后差等特点有关。随着对 信号传导途径研究的深入和更多靶向药物的出现,将会给TNBC的治疗带来更大的希望,从而进一步改善TNBC 患者的疗效和预后。并且,今后仍须努力寻找 更多可靠的分子生物学指标,进行分子病理分型和基因分型,指导治疗以及判断预后,从而改善TNBC患者生存。
作者:中国医学科学院肿瘤医院张灵小李慧慧徐兵河
上一篇:早期或重复暴漏于牙科X射线增加脑膜瘤发病风险
下一篇:2011消化道肿瘤领域:在创新中进步
论坛新帖
频道总排行
医学推广
频道本月排行
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(11)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)