是假性进展还是真的肿瘤复发?影像组学为你解忧!
2021-03-16 11:48:12 来源: 作者: 评论:0 点击:
关键字: 胶质母细胞瘤 | 复发性胶质母细胞瘤 | 纹理分析
在神经肿瘤学治疗反应评估(RANO)标准[1]中,确定对比增强肿瘤体积的程度是监测治疗反应的一个重要标志。现阶段已有多项研究表明,基于深度学习的自动分割(DLAS)技术可有效的评估治疗反应。无论是在日常实践还是在数据研究中,人工或半自动分割都需要大量的人力投入,然而DLAS技术可以节省时间并减少人力投入。DLAS技术有助于放射组学特征的再现,但它对放射组学建模的影响尚不明确。
近日,发表在European Radiology杂志的一项研究评价了DLAS提取MRI解剖和生理特征的能力,并比较了DLAS获得的放射组学特征与手动分割获得的放射组学特征所建立的放射组学模型诊断性能的差异,从而协助临床准确评价胶质母细胞瘤患者的治疗反应。
使用238例胶质母细胞瘤对DLAS模型进行训练,并在两所三级医院98例治疗前和86例治疗后的胶质母细胞瘤上进行来独立验证。从对比增强T1加权图像(CE-T1w)上提取1618个放射组学特征,从表观扩散系数(ADC)和脑血容量(CBV)mapping上提取直方图特征。使用来自受试者工作特征分析的曲线下面积(AUC)测试放射组学特征、ADC和CBV参数用于识别治疗反应的诊断性能。 使用0.80截止值来测试特征重现性,以得出一致性相关系数。
ADC和CBV特征(ICC, 0.82-0.99)以及一阶特征(治疗前和治疗后,剩余100%和94.1%)重现性较好,CE-T1w的纹理特征(剩余79.0%和69.1%)和小波变换特征(剩余81.8%和74.9%)的重现性较差。基于DLAS的放射组学在内部验证中表现出与人工分割相似的性能(AUC, 0.81 [95% CI, 0.64-0.99] vs. AUC, 0.81 [0.60-1.00],p = 0.80),但在外部验证中表现略低于人工分割(AUC, 0.78 [0.61-0.95] vs. AUC, 0.65 [0.46-0.84],p = 0.23)。
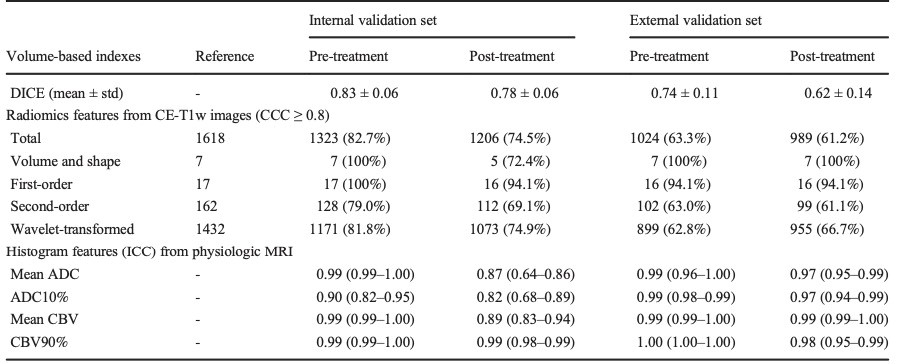
表1 基于深度学习的自动分割技术对治疗前、后胶质母细胞瘤解剖和生理MRI特征的影响。
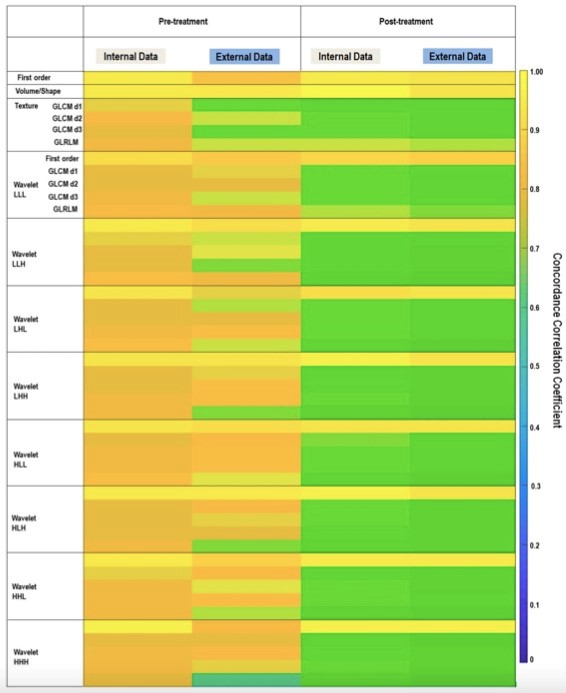
图1 DLAS提取的1618个放射学特征的一致性相关系数(CCC)的热图和参考的手动分割。在内部和外部验证中,纹理和小波特征以及治疗后的胶质母细胞瘤患者的特征再现性均较低。D,距离;GLCM,灰度共现矩阵;GLRLM,灰度游程矩阵;L,低通滤波器;H,高通滤波器。小波特征按一阶特征和纹理特征的顺序排列。
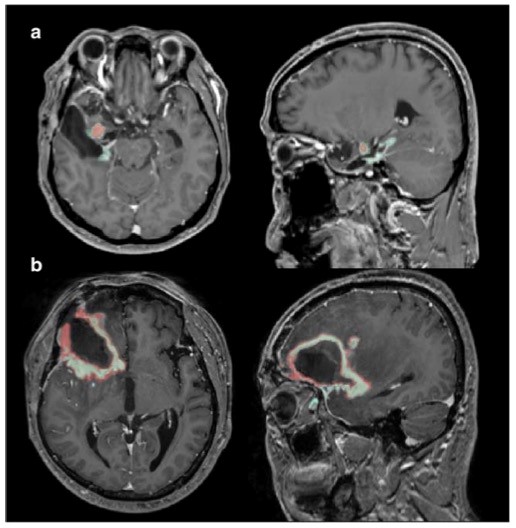
图2 治疗后胶质母细胞瘤中基于深度学习的自动分割(DLAS)的示例,其中出现假性进展(a)和肿瘤进展(b)。在治疗后的胶质母细胞瘤中,DLAS的分割精度(红色)低于作为参考的手动分割(绿色),尤其是假性进展伴有不确定性增强的病变时。
基于DLAS的特征提取对解剖和生理MRI的一阶特征具有较高的再现性,在识别假性进展方面的诊断性能可与人工手动分割相媲美,这支持DLAS在定量MRI分析中的应用。
原始出处:
Ji Eun Park,Sungwon Ham,Ho Sung Kim,et al. Diffusion and perfusion MRI radiomics obtained from deep learning segmentation provides reproducible and comparable diagnostic model to human in post-treatment glioblastoma.DOI:10.1007/s00330-020-07414-3
在神经肿瘤学治疗反应评估(RANO)标准[1]中,确定对比增强肿瘤体积的程度是监测治疗反应的一个重要标志。现阶段已有多项研究表明,基于深度学习的自动分割(DLAS)技术可有效的评估治疗反应。无论是在日常实践还是在数据研究中,人工或半自动分割都需要大量的人力投入,然而DLAS技术可以节省时间并减少人力投入。DLAS技术有助于放射组学特征的再现,但它对放射组学建模的影响尚不明确。
近日,发表在European Radiology杂志的一项研究评价了DLAS提取MRI解剖和生理特征的能力,并比较了DLAS获得的放射组学特征与手动分割获得的放射组学特征所建立的放射组学模型诊断性能的差异,从而协助临床准确评价胶质母细胞瘤患者的治疗反应。
使用238例胶质母细胞瘤对DLAS模型进行训练,并在两所三级医院98例治疗前和86例治疗后的胶质母细胞瘤上进行来独立验证。从对比增强T1加权图像(CE-T1w)上提取1618个放射组学特征,从表观扩散系数(ADC)和脑血容量(CBV)mapping上提取直方图特征。使用来自受试者工作特征分析的曲线下面积(AUC)测试放射组学特征、ADC和CBV参数用于识别治疗反应的诊断性能。 使用0.80截止值来测试特征重现性,以得出一致性相关系数。
ADC和CBV特征(ICC, 0.82-0.99)以及一阶特征(治疗前和治疗后,剩余100%和94.1%)重现性较好,CE-T1w的纹理特征(剩余79.0%和69.1%)和小波变换特征(剩余81.8%和74.9%)的重现性较差。基于DLAS的放射组学在内部验证中表现出与人工分割相似的性能(AUC, 0.81 [95% CI, 0.64-0.99] vs. AUC, 0.81 [0.60-1.00],p = 0.80),但在外部验证中表现略低于人工分割(AUC, 0.78 [0.61-0.95] vs. AUC, 0.65 [0.46-0.84],p = 0.23)。

表1 基于深度学习的自动分割技术对治疗前、后胶质母细胞瘤解剖和生理MRI特征的影响。

图1 DLAS提取的1618个放射学特征的一致性相关系数(CCC)的热图和参考的手动分割。在内部和外部验证中,纹理和小波特征以及治疗后的胶质母细胞瘤患者的特征再现性均较低。D,距离;GLCM,灰度共现矩阵;GLRLM,灰度游程矩阵;L,低通滤波器;H,高通滤波器。小波特征按一阶特征和纹理特征的顺序排列。

图2 治疗后胶质母细胞瘤中基于深度学习的自动分割(DLAS)的示例,其中出现假性进展(a)和肿瘤进展(b)。在治疗后的胶质母细胞瘤中,DLAS的分割精度(红色)低于作为参考的手动分割(绿色),尤其是假性进展伴有不确定性增强的病变时。
基于DLAS的特征提取对解剖和生理MRI的一阶特征具有较高的再现性,在识别假性进展方面的诊断性能可与人工手动分割相媲美,这支持DLAS在定量MRI分析中的应用。
原始出处:
Ji Eun Park,Sungwon Ham,Ho Sung Kim,et al. Diffusion and perfusion MRI radiomics obtained from deep learning segmentation provides reproducible and comparable diagnostic model to human in post-treatment glioblastoma.DOI:10.1007/s00330-020-07414-3
相关热词搜索:
上一篇:单细胞测序法为根治白血病开辟新途径
下一篇:弹性成像来鉴别胰腺癌与自身免疫性胰腺炎!
频道总排行
频道本月排行
热门购物
评论排行
- 2011年临床执业医师考试实践技能真...(13)
- 腋臭手术视频(12)
- 2008年考研英语真题及参考答案(5)
- 节食挑食最伤女人的免疫系统(5)
- 核辐射的定义和单位(5)
- CKD患者Tm与IMT相关(5)
- 齐鲁医院普外科开展“喉返神经监护...(5)
- windows7激活工具WIN7 Activation v1.7(5)
- 正常微循环(5)
- 美大学性教育课来真的 男女上阵亲...(4)